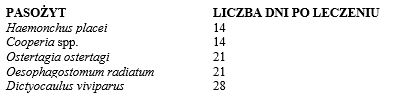Popularne tagi
bydło, cielęta, indyki, konie, koty, kozy, kury, lekarze, lisy, norki, nowości, owce, psy, warchlaki, świnie WszystkieMedimec Plus roztwór do wstrzykiwań
1. NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY
Podmiot odpowiedzialny i wytwórca odpowiedzialny za
zwolnienie serii:
Chanelle Pharmaceuticals Manufacturing Ltd.
Loughrea, Co. Galway, Irlandia
2. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
Medimec Plus roztwór do wstrzykiwań
3. ZAWARTOŚĆ SUBSTANCJI CZYNNEJ (-CH) I INNYCH SUBSTANCJI
Każdy ml klarownego, bezbarwnego do jasnożółtego
roztworu zawiera:
Substancje czynne:
Iwemektyna 10 mg/ml, Klorsulon 100 mg/ml
4. WSKAZANIA LECZNICZE
Produkt leczniczy weterynaryjny jest wskazany do leczenia mieszanych infestacji dorosłych przywr wątrobowych, nicieni żołądkowo jelitowych, nicieni płucnych, nicieni oczu i/lub roztoczy i wszy występujących u bydła mięsnego i bydła mlecznego nie produkującego mleka przeznaczonego do spożycia przez ludzi, gatunków wymienionych poniżej:
Ten produkt leczniczy weterynaryjny może być także stosowany jako pomoc w zwalczaniu inwazji wszołów (Damalinia bovis) i świerzbowców Chorioptes bovis, ale może nie nastąpić całkowite wyeliminowanie tych pasożytów.
DZIAŁANIE PRZEDŁUŻONE
Gdy bydło wypasane jest na pastwisku skażonym inwazyjnymi larwami nicieni, leczenie produktem w zalecanej dawce 1ml na 50 kg masy ciała kontroluje wystąpienie ponownej infekcji następujących pasożytów przez wymieniony okres:
5. PRZECIWWSKAZANIA
Nie podawać domięśniowo ani dożylnie.
Ten produkt przeznaczony jest tylko do stosowania u bydła. Nie stosować u innych gatunków gdyż mogą wystąpić ciężkie działania niepożądane włącznie ze śmiercią u psów (szczególnie u psów rasy collie, owczarków staroangielskich, ras pokrewnych oraz krzyżówek tych ras).
Nie stosować u zwierząt ze znaną nadwrażliwością na substancje czynne lub na dowolną substancję pomocniczą.
6. DZIAŁANIA NIEPOŻĄDANE
U niektórych zwierząt, w bardzo rzadkich przypadkach obserwowano po podaniu podskórnym przemijający dyskomfort. W bardzo rzadkich przypadkach może wystąpić obrzęk tkanek miękkich w miejscu iniekcji. Te reakcje ustępują bez leczenia.
Częstotliwość występowania działań niepożądanych przedstawia się zgodnie z poniższą regułą:
- bardzo często (więcej niż 1 na 10 leczonych zwierząt wykazujących działanie(a) niepożądane)
- często (więcej niż 1, ale mniej niż 10 na 100 leczonych zwierząt)
- niezbyt często (więcej niż 1, ale mniej niż 10 na 1000 leczonych zwierząt)
- rzadko (więcej niż 1, ale mniej niż 10 na 10000 leczonych zwierząt)
- bardzo rzadko (mniej niż 1 na 10000 leczonych zwierząt włączając pojedyncze raporty).
Można również zgłosić działania niepożądane poprzez krajowy system raportowania (www.urpl.gov.pl)
7. DOCELOWE GATUNKI ZWIERZĄT
Bydło
8. DAWKOWANIE DLA KAŻDEGO GATUNKU, DROGA (-I) I SPOSÓB PODANIA
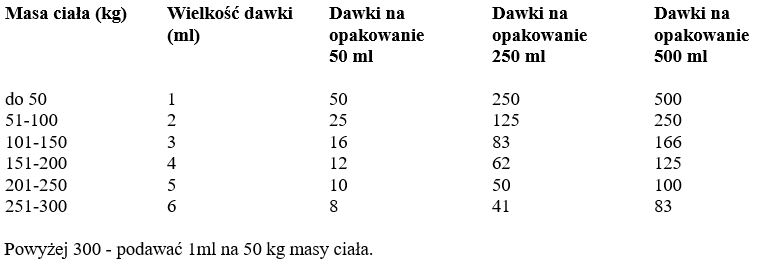
Produkt leczniczy weterynaryjny należy podawać wyłącznie poprzez iniekcję podskórną w oparciu o zalecaną dawkę 200 mcg iwermektyny i 2 mg klorsulonu na kg masy ciała. Każdy ml zawiera 10 mg iwermektyny i 100 mg klorsulonu, co wystarcza do leczenia zwierząt, których masa ciała wynosi 50 kg. Należy stosować następujący schemat dawkowania:
PODAWANIE:
Produkt leczniczy weterynaryjny należy podawać WYŁĄCZNIE PODSKÓRNIE. Wstrzyknąć w fałd luźnej skóry za łopatką. Zaleca się stosowanie sterylnych igieł o rozmiarze 17 (15-20 mm). Dla opakowania 50 ml zaleca się używanie strzykawki wielodawkowej. Ustalenie terminu leczenia należy oprzeć na czynnikach epidemiologicznych i indywidualnie dostosować go do każdego gospodarstwa. Program dawkowania powinien zostać opracowany przez wykwalifikowanego profesjonalistę. Aby zapewnić właściwe dawkowanie masę ciała należy określić najdokładniej jak to możliwe; należy sprawdzić precyzję dawkowania urządzenia dozującego. Jeśli zwierzęta będą leczone zbiorowo, to aby uniknąć podania zbyt niskiej dawki lub przedawkowania, należy je podzielić na grupy zgodnie z masą ciała i podać odpowiednią dawkę.
Nie jest zalecane przeprowadzanie iniekcji u zwierząt z mokrą lub brudną okrywą włosową.
W przypadku użycia strzykawki do iniekcji podskórnych należy zastosować igłę automatycznie pobierającą produkt z opakowania. Przy temperaturze produktu wynoszącej poniżej 5ºC mogą wystąpić trudności w podaniu wynikające ze zwiększonej lepkości. Ogrzanie produktu i sprzętu do iniekcji do temperatury około 15°C znacznie zwiększy łatwość podania produktu. Należy podawać w inne miejsca niż te, w które podano inne leki parenteralne.
Ten produkt nie jest przeznaczony do podawania dożylnego lub domięśniowego.
SPOSÓB DZIAŁANIA
Iwermektyna paraliżuje i ostatecznie zabija pasożytnicze nicienie, pajęczaki i owady, włączając gzy, przez wpływ na układ nerwowy pasożytów. W dawkach leczniczych iwermektyna nie wywiera szkodliwego wpływu na bydło, ponieważ nie przenika łatwo do ośrodkowego układu nerwowego. Iwermektyna należy do klasy awermektyn z grupy endektocydów o działaniu przeciwrobaczym. Sposób działania wykazywany przez awermektyny jest unikalny dla tej klasy produktów przeciwrobaczych. Klorsulon działa poprzez przerwanie metabolicznej aktywności przywry wątrobowej i hamowanie enzymów niezbędnych do produkcji energii.
9. ZALECENIA DLA PRAWIDŁOWEGO PODANIA
INSTRUKCJA STOSOWANIA Z UŻYCIEM
AUTOMATYCZNEGO SPRZĘTU DO INIEKCJI
• Przed użyciem zdezynfekować wszystkie igły i strzykawki poprzez gotowanie w czystej wodzie przez 15-20 minut
• Wygotowane igły przed użyciem należy przechowywać w antyseptycznym roztworze. Podczas iniekcji bydła należy je często wymieniać.
• Zaleca się użycie sterylnego sprzętu do pobierania produktu. Należy unikać zanieczyszczenia.
• Dokładnie podłączyć plastikową rurkę do strzykawki dozującej. W razie potrzeby użyć przejściówki
• Zdjąć korek z butelki i zdezynfekować gumowy korek alkoholem lub innym odpowiednim chemicznym środkiem dezynfekującym. Trzymać butelkę pionowo i całkowicie włożyć igłę do pobierania w środek gumowego korka. Pewnie zamocować za pomocą zakręcanej nasadki załączonej do rurki.
• Zawiesić odwróconą butelkę na szyi, ramieniu lub pasku.
• Delikatnie wstrząsnąć wstrzykiwacz. Sprzęt jest teraz gotowy do użytku.
• Po użyciu usunąć sprzęt do pobierania i przepłukać czystą wodą cały aparat przed odłożeniem do przechowania.
• Przechowywać częściowo zużytą butelkę w pudełku, w celu ochrony przed światłem. Nie używać ponownie pustych butelek.
• Jeśli rurka łącząca zostanie użyta po raz drugi, powinna być również, wraz ze strzykawką i igłami, gotowana przez 15-20 minut przed użyciem.
10. OKRES(-Y) KARENCJI
Okres karencji:
Tkanki jadalne - 66 dni
Produkt niedopuszczony do stosowania u zwierząt produkujących mleko przeznaczone do spożycia przez ludzi.
11. SPECJALNE ŚRODKI OSTROŻNOŚCI PODCZAS PRZECHOWYWANIA
Nie używać tego produktu leczniczego weterynaryjnego po upływie terminu ważności podanego na etykiecie i pudełku tekturowym po upływie terminu ważności. Termin ważności oznacza ostatni dzień danego miesiąca. Okres ważności po po pierwszym otwarciu opakowania bezpośredniego: 28 dni.
Przechowywać pojemnik w zewnętrznym opakowaniu tekturowym w celu ochrony przed światłem.
Wyłącznie dla zwierząt
Przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
12. SPECJALNE OSTRZEŻENIA
Po pobraniu pierwszej dawki produkt należy zużyć w ciągu 28 dni. Wyrzucić niezużyte materiały. Ten produkt nie zawiera żadnych środków konserwujących.
Przed pobraniem każdej dawki należy przetrzeć korek środkiem dezynfekcyjnym. Jeśli wystąpi jakaś widoczna wada lub odbarwienie, produkt należy wyrzucić.
Oporność na iwermektynę odnotowano u bydła dla Ostertagia ostertagi i gatunków Cooperia na terenie Unii Europejskiej. W związku z tym stosowanie tego produktu powinno być oparte na lokalnych (regionalnych, w danym gospodarstwie) danych epidemiologicznych na temat wrażliwości tych gatunków pasożytów oraz zaleceniach jak ograniczyć dalszą selekcję w kierunku rozwoju oporności na środki przeciwrobacze.
Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom:
Nie jeść, nie pić, nie palić w czasie pracy z produktem. Unikać bezpośredniego kontaktu produktu ze skórą. Po użyciu umyć ręce. Zachować ostrożność aby uniknąć przypadkowej samoiniekcji; produkt może spowodować miejscowe podrażnienie i/lub ból w miejscu iniekcji. Po przypadkowej samoiniekcji, należy niezwłocznie zwrócić się o pomoc lekarską oraz przedstawić lekarzowi ulotkę informacyjną lub opakowanie. Po przypadkowym kontakcie produktu ze skórą należy niezwłocznie umyć wodą z mydłem dotknięty obszar.
Po przypadkowym kontakcie produktu z oczami należy niezwłoczne przepłukać je wodą.
Należy uważać, aby nie stosować następujących praktyk, ponieważ zwiększają one ryzyko rozwinięcia się oporności i mogą być przyczyną nieskuteczności terapii
• Zbyt częste i powtarzające się stosowanie przez dłuższy okres czasu produktów przeciwrobaczy należących do tej samej klasy
• Stosowanie zbyt niskich dawek w wyniku niedoszacowania masy ciała, nieprawidłowe podanie produktu, brak kalibracji urządzenia dozującego (jeżeli ma zastosowanie)
W przypadku podejrzenia oporności na produkty przeciwrobacze należy przeprowadzić odpowiednie testy (np. test redukcji liczby wydalanych jaj w kale). W przypadku gdy rezultaty testów wskazują na silną oporność na dany produkt przeciwrobaczy należy zastosować lek należący do innej klasy farmakologicznej i charakteryzujący się odmiennym działaniem.
W celu uniknięcia reakcji wtórnych w związku ze śmiercią larw Hypoderma w przełyku lub kręgosłupie/rdzeniu kręgowym, zaleca się podawanie produktu na koniec okresu aktywności much
i przed dotarciem przez larwy na miejsca spoczynku; należy zasięgnąć profesjonalnej porady na temat odpowiedniego terminu leczenia.
Ten produkt jest bardzo toksyczny dla organizmów wodnych i żuków koprofagicznych. Leczone bydło nie powinno mieć bezpośredniego dostępu do stawów, strumieni czy kanałów przez 14 dni po leczeniu. Nie można wykluczyć długofalowego wpływu na żuki koprofagiczne wywołanego przez stałe lub powtarzane stosowanie produktu. W związku z tym powtarzane leczenie zwierząt na pastwisku, w ciągu sezonu, produktem zawierającym iwermektynę należy stosować tylko w przypadku braku alternatywnego leczenia lub możliwości zapewnienia utrzymania zdrowia zwierzęcia/stada, zgodnie z zaleceniami lekarza weterynarii.
Awermektyny mogą nie być dobrze tolerowane u nie docelowych gatunków zwierząt. Przypadki nietolerancji skutkujące śmiercią odnotowano u psów, szczególnie u psów rasy collie, owczarków staroangielskich, ras pokrewnych oraz krzyżówek tych ras i również u żółwi/żółwiaków.
Podzielić dawki przekraczające 10 ml na różne miejsca iniekcji i podać je w inne miejsca, niż te, w które podano inne produkty parenteralne.
Przetrzeć środkiem dezynfekcyjnym korek przed pobraniem każdej dawki. Unikać zanieczyszczenia podczas stosowania.
Przy stosowaniu opakowania 250 ml i 500 ml należy używać tylko strzykawek automatycznych.
Dla opakowania 50 ml zaleca się używanie strzykawki wielodawkowej.
Produkt może być podawany krowom mięsnym na każdym etapie ciąży lub laktacji pod warunkiem, że mleko nie jest przeznaczone do konsumpcji przez ludzi. Produkt nie wpływa na płodność krów i byków i może być podawany zwierzętom w każdym wieku włączając młode cielęta.
Nie zidentyfikowano interakcji z innymi produktami.
Podanie 5 ml na 50 kg masy ciała (pięciokrotność zalecanej dawki) może spowodować wystąpienie zmian w miejscu iniekcji (włączając obrzęk, nadwrażliwość i stan zapalny)
Nie jest spodziewane wystąpienie innych reakcji niepożądanych związanych z podaniem produktu.
Ponieważ nie wykonywano badań dotyczących zgodności, tego produktu leczniczego weterynaryjnego nie wolno mieszać z innymi produktami leczniczymi weterynaryjnymi.
13. SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO WETERYNARYJNEGO LUB POCHODZĄCYCH Z NIEGO ODPADÓW, JEŚLI MA TO ZASTOSOWANIE
NIEZWYKLE NIEBEZPIECZNY DLA RYB I ORGANIZMÓW WODNYCH.
Nie zanieczyszczać produktem ani zużytymi opakowaniami
wód powierzchniowych i kanałów. Niewykorzystany produkt leczniczy weterynaryjny lub jego odpady należy usunąć w sposób zgodny z obowiązującymi przepisami.
14. DATA ZATWIERDZENIA LUB OSTATNIEJ ZMIANY TEKSTU ULOTKI.
05.12.2018
15. INNE INFORMACJE
50, 250 lub 500 ml
Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
W celu uzyskania informacji na temat niniejszego produktu leczniczego weterynaryjnego, należy kontaktować się z lokalnym przedstawicielem podmiotu odpowiedzialnego:
Polska
ScanVet Poland Sp. z o.o.
Skiereszewo
ul. Kiszkowska 9
62-200 Gniezno
tel. 61 426 49 20
Pozwolenie nr 2823/18